| Autor |
Nachricht |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1479
|
 Verfasst am: 09. Feb 2024 07:49 Titel: Evans Auxilliar Verfasst am: 09. Feb 2024 07:49 Titel: Evans Auxilliar |
 |
|
Hallo,
es handelt sich um die folgende Reaktion. Ich muss erklären, warum die Temperatur so klein ist und was als Nebenprodukt entsteht. Das Nebenprodukt habe ich, aber ich check nicht warum die Temperatur so klein ist. Hat da jemand eine Erklärung?
Und das Problem mit dem Speicher wird bald gelöst, also keine Sorgen, ich werde in Zukunft keine Anhänge mehr löschen.
| Beschreibung: |
|
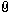
Download |
| Dateiname: |
52180C08-DD53-4175-B4E1-536289583D9D.jpeg |
| Dateigröße: |
59.19 KB |
| Heruntergeladen: |
249 mal |
|
|
 |
chemiewolf
Anmeldungsdatum: 06.07.2022
Beiträge: 583
Wohnort: Rheinhessen
|
 Verfasst am: 09. Feb 2024 09:18 Titel: Verfasst am: 09. Feb 2024 09:18 Titel: |
 |
|
je höher die Temperatur, desto größer die Wahrscheinlichkeit, dass Racemisierung auftritt, hier z.B. in alpha-Stellung zum Aldehyd
Zuletzt bearbeitet von chemiewolf am 09. Feb 2024 09:49, insgesamt 2-mal bearbeitet |
|
 |
OC-Gast
Gast
|
 Verfasst am: 09. Feb 2024 09:27 Titel: DIBAL Verfasst am: 09. Feb 2024 09:27 Titel: DIBAL |
 |
|
Mit DIBAL lassen sich verscheidene funktionelle Gruppen reduzieren.
Dabei können die Reaktivitäten und daraus sich ergebende Produkte unterschiedlich sein.
In der Regel werden Carbonsäurederivate(Ester,Nitrile,Amide..) mit DIBAL reduziert,wenn man zu den jeweiligen Aldehyden kommen will,eine Weiterreaktion ist unerwünscht.
Bei Estern und Amiden kann diese weitergehende Reduktion jedoch leicht erfolgen.Daher wird bei tiefen Temperaturen gearbeitet,wo die erste Reduktionsstufe mit DIBAL leicht erreicht wird.
Das dabei resultierend Zwischenprodukt ist weniger reaktiv(s. elektrophilen Charakter von DIBAL..).Geringere Reaktivität kann in der Chemie oft durch höhere Temperaturen ausgeglichen werden.Daher würde z.B. bei RT eine Reduktion mit DIBAL hier zum primären Alkohol führen,bei -55°C anscheinend nur in sehr geringem Maße.
OC-Gast.
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1479
|
 Verfasst am: 09. Feb 2024 09:43 Titel: Verfasst am: 09. Feb 2024 09:43 Titel: |
 |
|
|
Erstmal vielen Dank für eure Antworten, aber warum wird bei tiefen Temperaturen die erste Reduktionsstufe erreicht? Also warum entsteht bei höheren Temperaturen ein primärer Alkohol? Gibt es hierfür eine genaue Erklärung? Denn das versteh ich noch nicht.
|
|
 |
chemiewolf
Anmeldungsdatum: 06.07.2022
Beiträge: 583
Wohnort: Rheinhessen
|
 Verfasst am: 09. Feb 2024 09:48 Titel: Verfasst am: 09. Feb 2024 09:48 Titel: |
 |
|
|
besser als OC-Gast kann man da m.E. nicht erklären. Was ist denn noch unklar?
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1479
|
 Verfasst am: 09. Feb 2024 09:59 Titel: Verfasst am: 09. Feb 2024 09:59 Titel: |
 |
|
|
Ich versteh nur nicht warum bei tiefen Temperaturen dieses Produkt hier entsteht? Warum beeinflusst die Temperatur genau welches Produkt entsteht?
|
|
 |
chemiewolf
Anmeldungsdatum: 06.07.2022
Beiträge: 583
Wohnort: Rheinhessen
|
 Verfasst am: 09. Feb 2024 10:10 Titel: Verfasst am: 09. Feb 2024 10:10 Titel: |
 |
|
|
Das ist das Ergebnis von Forschungsarbeit. Bis diese Bedingungen bekannt waren, haben zig Doktoranden tausende Experimente gemacht....
|
|
 |
OC-Gast
Gast
|
 Verfasst am: 09. Feb 2024 11:25 Titel: Temperatur Verfasst am: 09. Feb 2024 11:25 Titel: Temperatur |
 |
|
| fragenstellen123 hat Folgendes geschrieben: | | Ich versteh nur nicht warum bei tiefen Temperaturen dieses Produkt hier entsteht? Warum beeinflusst die Temperatur genau welches Produkt entsteht? |
Das hat was mit der Aktivierungsenergie zu tun für die verschiedenen Reduktionsschritte.Je größer der Unterschied der AE,desto höher muß man mit der Temperatur gehen,um auch den zweiten Schritt zu erreichen.
Da die AE hier sich nicht so stark unterscheiden,würden bei Raumtemperatur bereits beide Reduktionsschritte ablaufen.
Daher arbeitet man bei ausreichend(empirisch ermitelt,s. chemiewolf) niedrigen Temperaturen,um diesen AE-Unterschied soweit zu nutzen,daß nur
die erste Reaktion abläuft.Dort ist dann die AE für die 2. Stufe zu hoch,um in größerem Maße zum Alkohol zu kommen.
OC-Gast.
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1479
|
 Verfasst am: 09. Feb 2024 13:54 Titel: Verfasst am: 09. Feb 2024 13:54 Titel: |
 |
|
Achso alles klar, danke dir OC-Gast!
Also man arbeitet mit tieferen Temperaturen, um zum Aldehyd zu gelangen, da sonst der primäre Alkohol entstehen würde. Im Grunde genommen entsteht auch bei tieferen Temperaturen primärer Alkohol, jedoch in geringeren Maßen. Um eben auf den Aldehyd zu kommen, muss mit niedrigeren Temperaturen gearbeitet werden. Also diese Begründung reicht so vollkommen aus, oder?
|
|
 |
chemiewolf
Anmeldungsdatum: 06.07.2022
Beiträge: 583
Wohnort: Rheinhessen
|
 Verfasst am: 09. Feb 2024 14:12 Titel: Verfasst am: 09. Feb 2024 14:12 Titel: |
 |
|
|
ja, passt
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1479
|
 Verfasst am: 10. Feb 2024 11:50 Titel: Verfasst am: 10. Feb 2024 11:50 Titel: |
 |
|
|
Danke!
|
|
 |
|