| Autor |
Nachricht |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 10:58 Titel: pH-Wert-Berechnungen Verfasst am: 05. März 2024 10:58 Titel: pH-Wert-Berechnungen |
 |
|
Hallo,
es handelt sich um die beiden Aufgaben (siehe Anhang). Habe ich die richtig berechnet. Bei der zweiten Aufgabe (19) ist irgendwas falsch. Ich habe versucht mit 2 verschiedenen Varianten zu rechnen, aber die Ergebnisse stimmen nicht überein. Was ist hier falsch? Beide Varianten machen irgendwie Sinn. Könnte jemand mal einen Blick werfen?
| Beschreibung: |
|
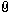
Download |
| Dateiname: |
E93A689E-D6BC-44C4-9B4F-64CB847BCABB.jpeg |
| Dateigröße: |
70.92 KB |
| Heruntergeladen: |
30 mal |
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6439
Wohnort: Berlin
|
 Verfasst am: 05. März 2024 12:29 Titel: Verfasst am: 05. März 2024 12:29 Titel: |
 |
|
18 ist richtig. Jedoch in der HH Gleichung kürzt sich das Volumen raus. Es reicht nur mit den Stoffmengen zu rechnen.
19. pkB und pks verwechselt. Eine Ammoniaklösung kann niemals sauer sein.
Für schwache Basen gilt
pOH = 0,5*(pkb- logcBase)
pOH =0,5 *(5-log(0,45))
pOH = 2,67
pH =14-pOH
pH = 11,33
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 13:48 Titel: Verfasst am: 05. März 2024 13:48 Titel: |
 |
|
|
Aber im Internet steht, dass der pH-Wert einer schwachen Base 14- 1/2*(pKB-log(c)) ist. Bin nun voll verwirrt. Warum kann ich das so nicht rechnen?
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6439
Wohnort: Berlin
|
 Verfasst am: 05. März 2024 13:50 Titel: Verfasst am: 05. März 2024 13:50 Titel: |
 |
|
|
Nichts anderes habe ich oben gerechnet
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 13:55 Titel: Verfasst am: 05. März 2024 13:55 Titel: |
 |
|
|
Achja sry, hatte grade einen Denkfehler. Vielen Dank für die Erklärung, habs jetzt gecheckt.
|
|
 |
|