| Autor |
Nachricht |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 24. Feb 2024 17:44 Titel: pH-Wert einer Benzoesäure-Lösung Verfasst am: 24. Feb 2024 17:44 Titel: pH-Wert einer Benzoesäure-Lösung |
 |
|
Hallo an alle,
es handelt sich um die folgende Aufgabenstellung (siehe Anhang). Wie ist man auf die Gleichung Ks gekommen? Ist die Rechnung überhaupt so richtig? Sollte man hier nicht die Handerson-Hasselbalch Gleichung verwenden? Ich kann nachvollziehen, wie man auf die Umformung Ks=x^2/c(Benzoesäure) kommt.
| Beschreibung: |
|
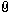
Download |
| Dateiname: |
C7508300-9901-4059-B3DB-A0E45E40CEC8.jpeg |
| Dateigröße: |
68.96 KB |
| Heruntergeladen: |
51 mal |
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 24. Feb 2024 21:04 Titel: Verfasst am: 24. Feb 2024 21:04 Titel: |
 |
|
pH schwacher Säure allgemein
pH = 1/2 · ( pK S - lg ( c ( HA ) )
Deine Rechnung zeigt die nicht logaritmierte Form.
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 24. Feb 2024 21:42 Titel: Verfasst am: 24. Feb 2024 21:42 Titel: |
 |
|
|
Alles klar, danke, aber wie ist man auf diese Umformung Ks=x^2/c(Benzoesäure) gekommen? Das check ich noch nicht.
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 24. Feb 2024 21:51 Titel: Verfasst am: 24. Feb 2024 21:51 Titel: |
 |
|
Reaktion ist
C6H5COOH => C6HCOO- + H+
Ks = cC6H5COO- * cH+/ cC6H5COOH
Da cH+ = cC6H5COO- = x ist
ergibt sich ks = x^2/cC6H5COOH
Der Rest in Deiner Aufgabe
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 24. Feb 2024 23:11 Titel: Verfasst am: 24. Feb 2024 23:11 Titel: |
 |
|
Das check ich noch nicht, warum ist cH+ = cC6H5COO- = x ?
Warum sind beide x?
Ist es nicht sowas wie:
............. C6H5COOH --> C6HCOO- + H+
A:............0,1 mol/L............0
GGW:.......0,1-x..................x.............x
Ks = x^2/ (0,1-x) ??
Ist diese Überlegung falsch?
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 25. Feb 2024 00:01 Titel: Verfasst am: 25. Feb 2024 00:01 Titel: |
 |
|
Das heißt doch nur aus einem Molekül Benzoesäure entsteht 1 Teilchen H+ und 1 Benzeoatteilchen. Also die Anzahl sind gleich, daher kann man Quadrieren.
Das Massenwirkungsgesetz für A => B + C ist
K = B*C/A
Die Differenz kommt erst zum Tragen, wenn man Gleichgewichte betrachtet.
Ja streng genommen müsste man so rechnen, wie Du es aufgeschrieben hast. Es kommt dann eine quadratische Gleichung raus.
Die Frage ist wie gross ist der Unterschied.?
0,000357 pH unterschied zu den 2,6. Also vernachlässigbar.
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 09:03 Titel: Verfasst am: 05. März 2024 09:03 Titel: |
 |
|
Vielen Dank für die Erklärung, aber wie bist du auf 0,000357 gekommen? Alsod u meintest ja es sei vernachlässigbar klein, wie finde ich das heraus? Hab's noch nicht ganz gecheckt..
Edit: Also was wäre x in diesem fall? Also 0,1 -x ? Was wäre dieses x?
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 05. März 2024 10:38 Titel: Verfasst am: 05. März 2024 10:38 Titel: |
 |
|
Löse die quadratische Gleichung doch mal.
Ks = x^2/ (0,1-x)
Nach x umstellen
Ks*(0,1-x)= x^2
Ks*0,1 - ks*x = x^2
f(x) = x^2 + Ks*x-0,1*ks
x1 = -ks/2+sqr((ks/2)^2 + 0,1*ks)
x2 = -ks/2 - sqr((ks/2)^2 + 0,1*ks)
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 14:58 Titel: Verfasst am: 05. März 2024 14:58 Titel: |
 |
|
|
Achso, das ist einfach das lösen einer quadratischen Gleichung. Für x kommt ein sehr geringer wert raus, weshalb wir -x sozusagen vernachlässigen können oder? Aber hätte ich auch irgendwie erkennen können, dass x klein ist, ohne jetzt die Gleichung quadratisch aufzulösen?
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 05. März 2024 15:42 Titel: Verfasst am: 05. März 2024 15:42 Titel: |
 |
|
Vergleiche die Ergebnisse
Man kann vereinfachen.
|
|
 |
fragenstellen123
Anmeldungsdatum: 19.02.2021
Beiträge: 1373
|
 Verfasst am: 05. März 2024 17:03 Titel: Verfasst am: 05. März 2024 17:03 Titel: |
 |
|
|
Wie meinst mit vereinfachen? pH ist ja 2,6 und die Konz. 0,1 M
|
|
 |
Nobby
Moderator
Anmeldungsdatum: 20.10.2014
Beiträge: 6440
Wohnort: Berlin
|
 Verfasst am: 05. März 2024 17:10 Titel: Verfasst am: 05. März 2024 17:10 Titel: |
 |
|
|
Setz dich mal hin und rechne die Quadratische Gleichung aus und Vergleiche mit dem Ergebnis der vereinfachten Form.
|
|
 |
|